Klinisk retningslinje: Hemodynamisk montering med bruk av PiCCO-systemet

Indikasjon
PiCCO-systemet brukes for utvidet hemodynamisk monitorering hos intensivpasienter der sirkulatorisk status ikke fullt ut kan vurderes ved bruk av kliniske parametere alene. Invasiv blodtrykksmålinger gi bare en svært usikkert vurdering av cardiac output (CO). Ingen absolutte indikasjoner eksisterer, men vurder PiCCO ved:
- Høy dose noradrenalin (NA) eller flere pressorer
- Betydelig behov for intravenøs væsketilførsel
- Vedvarende hemodynamisk ustabilitet til tross for initial behandling
- ARDS uten akutt høyre hjertesvikt
PiCCO gir omfattende innsikt i hjertets preload, kontraktilitet og afterload, og dermed en bedre forståelse av oksygentilbud (DiO₂). Ved å følge PiCCO-parametre kan behandling skreddersys for å opprettholde optimal sirkulasjon og oksygenering, men PiCCO verdien må alltid ses i sammenheng med andre kliniske sirkulajonsparameter, blodtrykk og ekko.
Ingen absolutte kontraindikasjoner, men følgende forhold må vurderes:
- Vaskulærtilgang: Unngå punktering av arteria femoralis ved tidligere vaskulær kirurgi (f.eks. femoral bypass, bukseprotese). Vurder arteria brachialis som et alternativ.
- Koagulopati: Er ikke en absolutt kontraindikasjon, men vurdering av trombocyttall, INR og APTT er nødvendig. Diskusjon med ansvarlig overlege kreves, og prioriter erfarne lege for punksjonen.
- Klaffepatologi og IABP: Alvorlig klaffepatologi og intra-aortaballongpumpe (IABP) påvirker PiCCO-målinger, og bruken bør derfor vurderes nøye. PiCCO verdier må brukes svært tilbakeholdende og alltid sammenlignes med andre hemodynamiske parameter og ekko.
- Høyre hjertesvikt: PiCCO måler kun global hjertefunksjon og skyller ikke mellom høyre og venstre hjerte for preload og kontraktilitet. Høyre hjertesvikt med redusert pumpefunksjon og dilatert høyre atrium / ventrikkel vil derfor gi et feil bildet av venstre ventrikkel preload og funksjon (GEDVI overestimert og VV funksjon underestimert)
Pasienter i sirkulatorisk sjokk krever ofte både væskeresuscitering og katekolaminer for å nå hemodynamiske mål. Kliniske parametere som hudfarge, temperatur, kapillærfyllingstid, hjertefrekvens og blodtrykk gir ikke alltid et fullstendig bilde av hemodynamisk status.
PiCCO gir en mer sammensatt vurdering av hjertets preload, kontraktilitet og afterload og kan dermed bidra til å optimalisere oksygentilbudet (DiO₂) i forhold til oksygenbehovet (VO₂). I tillegg gi PiCCO systemet et troverdig estimat av lungeødem som kan brukes i væskebehandling og behandling av ARDS.
På intensivavdelingen brukes PiCCO sammen med andre hemodynamiske indikatorer som laktat, ScvO₂, kliniske parametere og ekkokardiografi. PiCCO-målinger har vist seg å være likeverdige med transkardielle målinger (pulmonaliskateter) av cardiac output (CO), og på enkelte områder er de overlegne, f.eks. når det gjelder å estimere preload.
PiCCO-oppsett
- Kateterplassering: PiCCO-kateter plasseres fortrinnsvis i arteria femoralis (5 Fr, 20 cm) med bruk av ultralyd og sterilt utstyr. Alternativt kan arteria brachialis (4 Fr, 22 cm) benyttes. Unngå å plassere både SVK og PiCCO i samme lyske for å redusere risiko for cross-talk.
- Liggetid: PiCCO kateter må fjernes etter 10 dager, men kan brukes om vanlig arteriell kateter, hvis det er ikke behov for PiCCO målinger lengre
- Sentral venøs tilgang: Bør ideelt ha spissen i vena cava superior, men vena femoralis kan også benyttes. Ved SVK i V.femoralis ble GEDVI overestimert, måling av CI ble ikke påvirket
PiCCO-målinger og -parametere
PiCCO-systemet måler og analyserer kontinuerlig trykkbølgen fra arteriekateteret for å beregne kontinuerlig cardiac output (CCO) ved hjelp av pulskonturanalyse. For å sikre nøyaktighet i CCO-målingene kreves kalibrering med termodilusjon. CCO-målinger er pålitelige så lenge det ikke er endringer i vaskulær motstand (f.eks. økt pressorbehov) eller betydelige hemodynamiske variasjoner. Når CCO brukes til å evaluere behandlingseffekter, anbefales hyppige kalibreringer, opptil hver time. Ved stabile forhold, eller når CCO er mindre avgjørende, kan kalibreringsintervallene forlenges til opptil åtte timer. Generelt vil nøyaktigheten i de kontinuerlige målingene avta med økt tid siden siste kalibrering.
Indekserte parametere: I klinisk praksis anvendes primært indekserte verdier, som cardiac index (CI), for å gjøre verdiene uavhengige av pasientens høyde og vekt. Disse verdiene oppnås ved å relatere ikke-indekserte målinger til pasientens størrelse, for eksempel ved å beregne CI som CO delt på kroppsoverflateareal (BSA, body surface area). BSA brukes som mål for pasientens kroppsstørrelse.
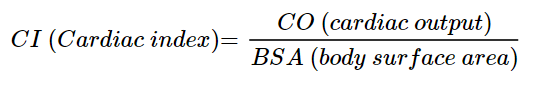
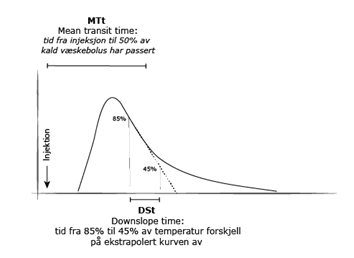
Kalibreringsprosessen: Ved termodilusjon injiseres kald væske i vena cava, og temperaturforandringen måles i arterien. PiCCO bruker følgende målinger for å beregne parametere:
- Areal under temperaturkurven: Beregner cardiac output (CO)
- Mean transit time (MTt): Gir intra-thoracic termovolum (ITTV)
- Downslope time (DST): Beregner pulmonal termisk volum (PTV)
Basert på disse målingene beregnes hemodynamiske parametere som gir informasjon om preload, kontraktilitet og afterload.
GEDVI (Global End-Diastolic Volume Index):
- Beregning og betydning: Reflekterer blodvolumet i begge hjertekamrene under diastolen. GEDVI kan brukes til å vurdere om cardiac index (CI) sannsynligvis vil respondere på økt preload (f.eks. ved væsketilførsel). GEDVI har en god relasjon til preload, men kan ikke forutse om ytterlige væsketilførelse vil føre til pulmonal stuvning (lungeødem).
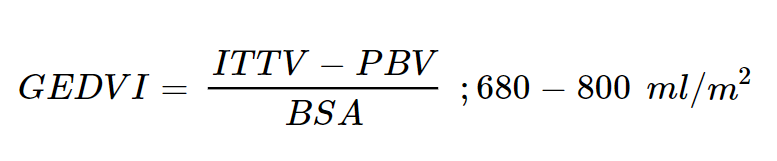
- Relasjon til CI: Økt preload gjennom væsketilførsel kan forbedre hjertets fylling, noe som kan øke CI og dermed DiO₂. Imidlertid betyr væskeresponsivitet ikke nødvendigvis at mer væske trengs; den hemodynamiske helheten må vurderes før væskeadministrasjon.
- Behandlingstiltak: Vurder væskebehandling dersom GEDVI er lav (< 800ml/m2) og kliniske tegn på hypoperfusjon eller lavt DiO₂ er tilstede. Unngå overvæsking da dette kan føre til lungeødem, sentral venøsstuvning og dårligere organperfusjon.
EVLWI (Extravascular Lung Water Index):
Beregning og betydning: EVLWI er en sensitiv indikator for lungeødem og øker før røntgen- eller blodgass vises tegn til lungeødem. EVLWI har en svært god korrelasjon til reel væskemengde i lungene og forandre seg i løpet av minutter ved akutt lungeødem (f.eks. ved weaning failure).
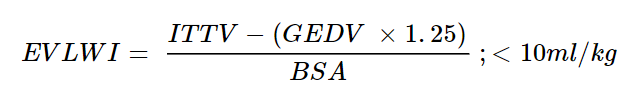
Relasjon til Preload EVLWI er ikke en direkte perload parameter, men kan hjelpe å vurdere om pasienten med redusert GEDVI er fortsatt væsketolerant. Høy EVLWI (> 10ml/kg) antyder væskeoverbelastning. Med hjelp av PVPI (pulmonary vascular permeablity index, forhold mellom intravasal og ekstravasal pulmonal væske), kan man skylle mellom kardiogent lungeødem (PVPI < 3) og permeablitets ødem (f.eks. ARDS, pneumoni) ved PVPI > 3.
Behandlingstiltak: Begrens væskeinntak hvis ELWI er høy, og vurder væsketrekk. Lav EVLWI krever ingen tiltak. Differensiering av lungeødem basert på PVPI bør bekreftes med ekko.
SVV (Stroke Volume Variation):
Beregning og betydning: Viser variasjon i slagvolumet under respirasjon, og en høy SVV indikerer væskeresponsivitet, spesielt hos intuberte og kontrollert ventilerte pasienter med sinusrytme. Fordelen med SVV er at det er en dynamisk parameter som forandre seg umiddelbart ved forandring av preload, f.eks. vil en passiv leg raise eller begrenset væskebolus gi umiddelbart effekt på SVV.
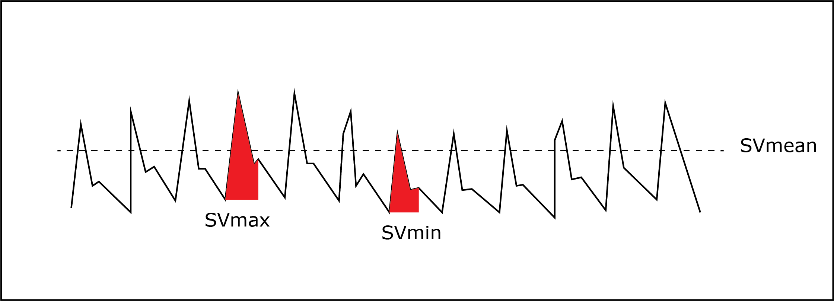
Relasjon til CI: Høy SVV kan indikere redusert preload og en økning av preload (f.eks. væske) kan forbedre CI og dermed øke DiO₂.
Behandlingstiltak: Vurder væskeadministrasjon hvis SVV er høy, men SR og er mekanisk ventilasjon er forutsetninger for sikkert tolkning av SVV.
CI (Cardiac Index):
Beregning og betydning: Angir mengden blod pumpet per minutt per kvadratmeter kroppsoverflate. CI reflekterer hjertets evne til å møte kroppens O₂-behov og er den viktigste parameteren for oksygentilbud (DiO₂).
Relasjon til DiO₂ og VO₂: Lav CI gir redusert DiO₂, noe som kan føre til organisk hypoksi, hvis O2 behovet (VO2) er større en DiO2. I situasjoner med høyt metabolsk behov (høy VO₂) som traumer eller sepsis, kan det være behov for CI > 3,0 L/min/m² for å opprettholde adekvat DiO₂, mens andre pasienter (sedert og ventilert) kan har en adekvat DiO2 med CI < 3.0 L/min/m2.
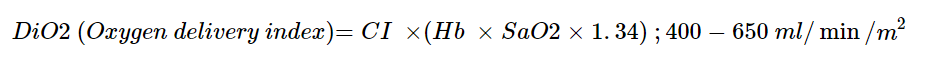
Behandlingstiltak: Øk CI ved tegn på organsvikt og lav DiO₂ (høy laktat, lav ScvO2, høy dpCO2, forlenget kapillær fyllingstid) ved hjelp av optimaliser preload, inotrope midler eller redusert afterload. Vurdere å redusere VO2 med hjelp av økt sedering eller kontrollert, invasiv ventilasjon.
SI (Stroke Volume Index):
Beregning og betydning: Volumet av blod pumpet per hjerteslag per kvadratmeter kroppsoverflate. Høy SI indikerer god kontraktilitet og tilstrekkelig preload.
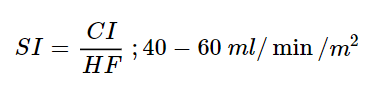
Relasjon til CI: Optimal SI bidrar til adekvat DiO₂ ved å sikre god slagvolum og CI. Ved redusert SI kan redusert CI kompenseres med økning av hjertefrekvens.
Behandlingstiltak: Ved lav SI, vurder å forbedre preload eller kontraktilitet gjennom væske eller inotropi, avhengig av samtidig måling av GEDVI,SVRI, dPmax og ekko.
dPmax
Beregning og betydning: Vurderer venstre ventrikkels kontraktilitet basert på brattheten til arteriekurven i systolen. En bratt stigning tilsier god ventrikkelfunksjon.
Relasjon til CI: Høy dPmax indikerer god kontraktilitet. Lav dPmax (< 1200mmHg/sec) kan indikere behov for inotrope støtte.
Behandlingstiltak: Ved lav dPmax, redusert CI og tegn på organsvikt, vurder inotrope midler for å forbedre kontraktilitet.
GEF og CFI
Beregning og betydning: Begge parameter gi estimat av venstre ventrikkel funksjon og er kontraktilitetsparameter. GEF (global ejection fraction) gir et uttrykk for hjertets samlede ejectjonsfraksjon og brukes som et globalt mål for hjertets kontraktilitet. CFI (Cardiac function index) tar hensyn til både hjertevolum og tidsaspektet, og kan gi en mer omfattende vurdering av hjertets totale pumpekapasitet enn GEF alene. Begge parameter har noen begrensinger og gjenspeile LVEF dårligere en ekko.
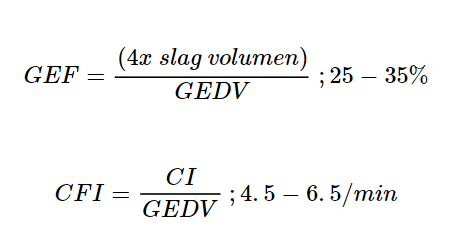
Relasjon til CI: Lav GEF og CFI er relatert til redusert LVEF og forandring i disse verdiene krever en ekko for å bekreft mistanke om reduser venstre ventrikkel funksjon. Nedsatt LVEF (ekko, GEF, CFI) gir en redusert CI og trenger tiltak ved tegn til organsvikt.
Behandlingstiltak: GEF / CFI skal anses overvåkningsparameter og en fall i disse verdiene burde utløse en nærmere undersøkelse av VV med ekko.
3. Afterload-parametere
SVRI (Systemic Vascular Resistance Index):
Beregning og betydning: Beskriver den systemiske vaskulære motstanden, avhengig av middelarterietrykk (MAP) og CI. Høy SVRI kan påvirke CI ved å endre hjertets arbeidsbyrde.
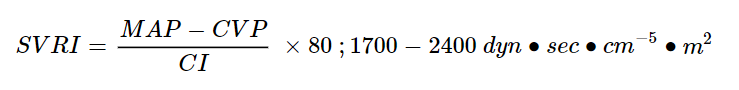
Relasjon til CI: Høy SVRI kan øke hjertets oksygenbehov (VO₂), mens lav SVRI kan gi suboptimal MAP for organperfusjon. Balanser SVRI for å optimalisere perfusjon uten å øke hjertets arbeidsbelastning for mye.
Behandlingstiltak: Juster av behandling etter SVRI burde kun gjøres med forsikt og med å ta hensyn på andre hemodynamsike parameter. Reduksjon av afterload med vasodilaterende midler kan forbedre CI men adekvat perfussjonstrykk med opprettholdes.
Mekanisk sirkulasjonsstøtte (MCS): Ved bruk av intra-aortaballongpumpe (IABP), ECMO eller Impella, kan PiCCO-målinger betydelig bpåvirkes og PiCCO parameter er ikke validert ved bruk av MCS. Unngå styring av behandlingen etter PiCCO under slike forhold.
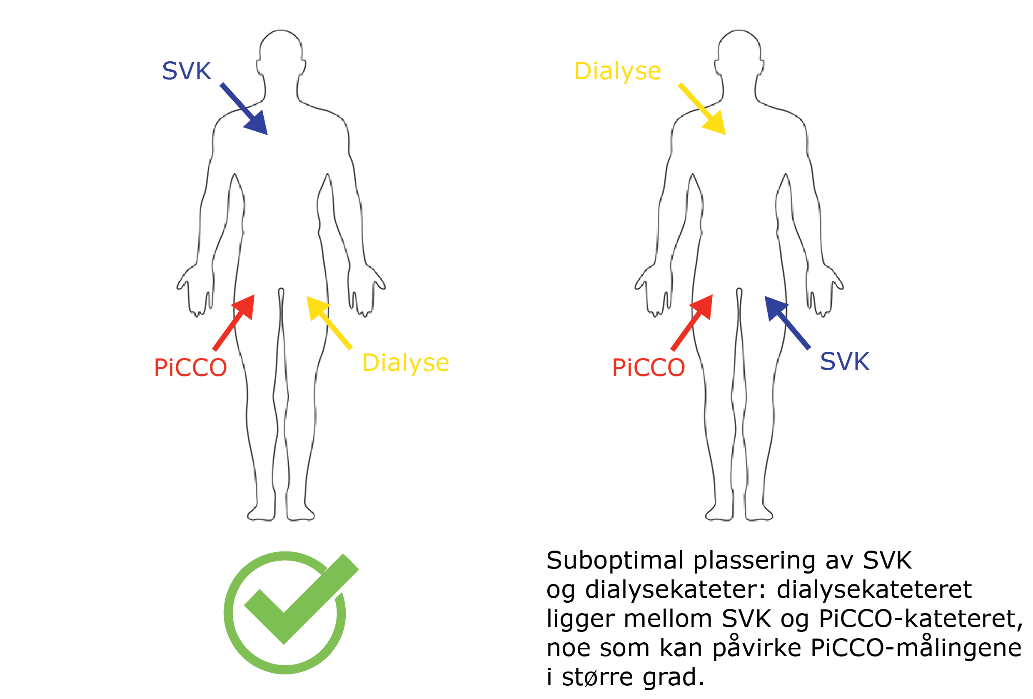
Dialyse: Bruk av dialyse er mulig og påvirke PiCCO målinger i mindre grad. Ideelt sett bør dialysekateter ikke plasseres mellom SVK og arteriekateter, da dette kan føre til en sterkere underestimering av CI og GEDVI. Hvis dialysekateteret er plassert suboptimalt, kan PiCCO-målinger fortsatt være mulige, men verdiene kan bli mer påvirket av dialysen enn ved optimal plassering. Når dialyseinnstillingene forblir relativt uendret, kan man sammenligne forskjellige målinger, men det kan være avvik fra verdiene som ble målt før dialysen ble startet.
Høyresidig hjertesvikt, alvorlig klaffepatologi, patologisk pulmonal sirkulasjon: Bruk av PiCCO kan være utfordrende og krever ekstra vurdering. Høyre hjertesvikt og alvorlig klaffepatologi (særlig klaffelekasje) gi en feil vurdering av venstre ventrikkelfunksjon og preload. Patologisk pulmonal sirkulasjon (pulmektomi, lobektomi, stor lungeemboli, store mengder pleuravæske) påvirker ELWI målinger.
MR: PiCCO kateteret inneholde metall og må fjernes før MR for å unngå pasientskader og artefakter.
Kilder
Monnet, X., Teboul, JL. Transpulmonary thermodilution: advantages and limits. Crit Care 21, 147 (2017).
Bendjelid, Karim et al. “Validation of a new transpulmonary thermodilution system to assess global end-diastolic volume and extravascular lung water.” Critical care 14,6 (2010): R209.
Michard F, Alaya S, Zarka V, Bahloul M, Richard C, Teboul JL. Global end-diastolic volume as an indicator of cardiac preload in patients with septic shock. Chest. 2003;124(5):1900–8.
Bercker S., Laudi S., Kaisers U.X., 2016, Intensivmedizin konkret: Fragen und Antworten, 1. Ediiton, Deutscher Ärzte Verlag, Köln.
Stiebel H.W., 2014, Die Anästhesie, 3. Edition, Schattauer, Stuttgart
https://derangedphysiology.com/
https://www.getinge.com/de/produkte/picco/